Novavax é uma empresa de biotecnologia sediada em Maryland que está adotando uma abordagem tradicional para desenvolver uma vacina contra a doença coronavírus 2019 (COVID-19). A empresa iniciou um teste de Fase 3 de sua vacina candidata, NVX ‑ CoV2373, no Reino Unido em setembro e um segundo teste de Fase 3 nos Estados Unidos e no México em dezembro. Esses dois testes em estágio final irão inscrever um total combinado de cerca de 45.000 participantes.
Embora isso coloque a Novavax atrás de seus concorrentes, os resultados iniciais de seus testes de vacinas são promissores.
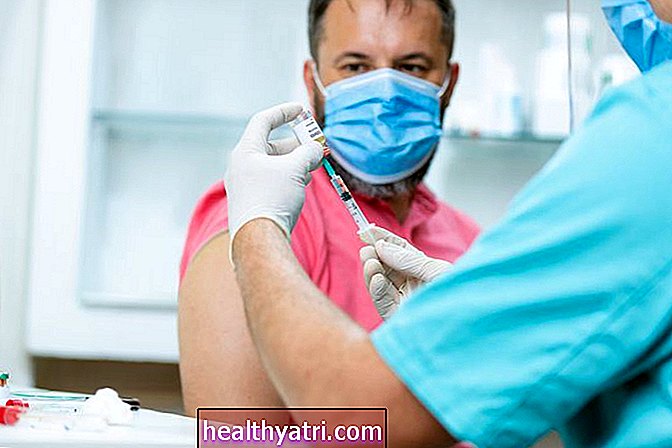
zoranm / Getty ImagesComo funciona
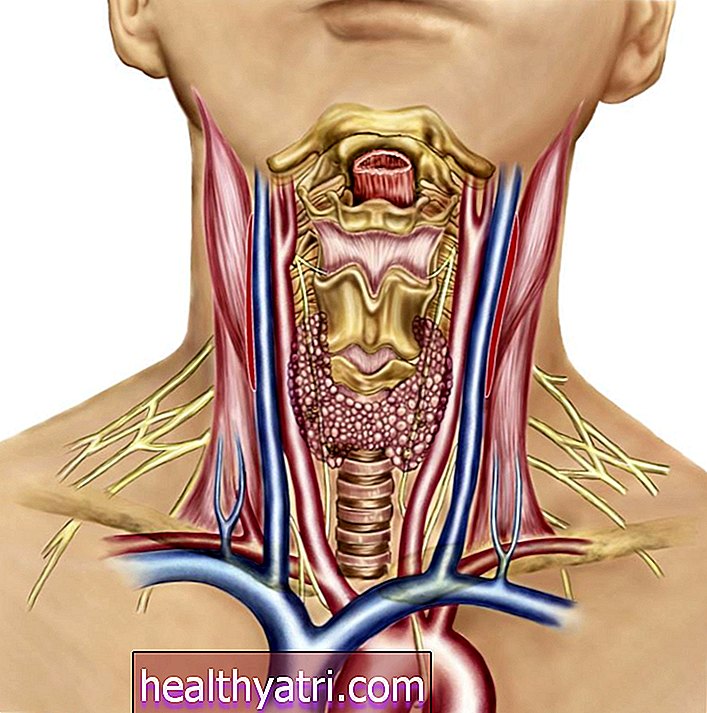
A vacina Novavax usa uma proteína de pico feita sob medida que imita a proteína de pico natural do novo coronavírus. A Novavax trabalhou durante anos no desenvolvimento de sua tecnologia de nanopartículas recombinantes e criou a primeira vacina COVID-19 usando esse método na primavera. No verão, os primeiros testes clínicos mostraram que a vacina parecia ser segura, e testes mais avançados entraram em fase de planejamento nos Estados Unidos e em outros países.
A vacina de duas doses funciona introduzindo uma proteína que estimula uma resposta do anticorpo, que bloqueia a capacidade do futuro coronavírus de se ligar às células humanas e prevenir a infecção. A proteína é combinada com o adjuvante Matrix-M da Novavax, que é importante para aumentar a resposta imune induzida pelo antígeno da proteína.
Quão eficaz é isso?
Os primeiros resultados de testes de vacinas publicados pela Novavax revelaram uma forte resposta de anticorpos à vacina em animais. Em agosto de 2020, os primeiros testes em humanos mostraram fortes respostas de anticorpos sem eventos adversos graves e poucos efeitos colaterais.
No final de janeiro, a Novavax anunciou que uma análise preliminar de dados de seu ensaio de Fase 3 no Reino Unido mostrou que a vacina era 89,3% eficaz e incluía proteção contra a variante B.1.1.7 do Reino Unido. A empresa também anunciou que a vacina foi 60% eficaz em um ensaio clínico de Fase 2b na África do Sul e incluiu proteção contra a variante sul-africana B.1.351.
Os resultados de todos os ensaios clínicos em estágio avançado são esperados em 2021.
No ensaio da Novavax, os participantes não serão expostos diretamente ao vírus, mas em vez disso, os pesquisadores usarão uma abordagem de infecção natural. O desafio será determinar se a vacina ou outras medidas de proteção, como mascaramento ou distanciamento social, oferecem a maior proteção.
Quando estará disponível?
A vacina candidata da Novavax está gerando muito interesse porque os primeiros dados de estudos em animais mostraram que ela era altamente eficaz na prevenção da replicação do coronavírus nas vias nasais. É um desenvolvimento importante para as vacinas COVID, pois pode ajudar a reduzir as taxas de infecção e transmissão . Embora isso ainda não tenha sido estabelecido em estudos humanos.
No entanto, a Novavax está atrás de seus concorrentes quando se trata de testes clínicos, portanto, mesmo que continue a ter bom desempenho nos testes, a vacina pode não estar disponível até o final de 2021. A empresa ainda não divulgou nenhuma estimativa sobre as datas de distribuição. A própria empresa também enfrenta um desafio significativo, pois 2019 foi um ano difícil para a Novavax.CiênciaA revista relatou que a empresa vendeu algumas de suas instalações de fabricação e tem que contar com mais empreiteiros para fabricar muitas de suas vacinas. Isso pode resultar em um atraso na produção.
Nenhuma informação foi fornecida ainda sobre o preço da vacina.
Vacinas COVID-19: Mantenha-se atualizado sobre quais vacinas estão disponíveis, quem pode obtê-las e quão seguras são.
Quem pode obter a vacina Novavax?
Como outras vacinas candidatas COVID-19, a vacina Novavax foi testada em adultos com 18 anos ou mais. A empresa não forneceu atualizações sobre testes em crianças e adolescentes. Ainda não foram fornecidas informações sobre as preocupações de grupos específicos.
Independentemente das populações do grupo de estudo, quem pode receber as vacinas COVID será em grande parte uma decisão regulatória feita pela Food and Drug Administration (FDA). A elegibilidade durante a distribuição será então determinada em nível estadual e pelos Centros de Controle e Prevenção de Doenças (CDC).
O CDC está liderando os esforços de vacinação e todos os pedidos da vacina COVID-19, independentemente do fabricante, passarão pela agência. O CDC também está supervisionando a distribuição de vacinas. O Comitê Consultivo sobre Práticas de Imunização (ACIP) do CDC fez recomendações sobre como priorizar o fornecimento de vacinas.
Os profissionais de saúde e as pessoas que vivem em instituições de longa permanência foram os primeiros a receber as vacinas COVID-19 autorizadas. De acordo com o CDC, há mais de 18 milhões de profissionais de saúde nos Estados Unidos e cerca de 1,3 milhão de americanos vivendo em instituições de longa permanência. Cada uma dessas pessoas precisaria receber duas doses das vacinas autorizadas até aqui.
O CDC estimou que levará vários meses antes que o fornecimento de vacinas atenda à demanda. Orientação sobre quem receberá a vacina e quando será decidido assim que os suprimentos estiverem disponíveis. Os Estados Unidos sozinhos têm uma população de cerca de 330 milhões - o que significa que quase 700 milhões de doses de vacina serão necessárias para vacinar toda a América se outras vacinas seguirem uma dose de duas vacinas.
Embora haja pouca informação disponível sobre os detalhes de quando todos receberão as vacinas e onde podem obtê-las, as secretarias estaduais e locais de saúde estarão coordenando esforços para distribuir as doses das vacinas assim que estiverem disponíveis. A vacina deve estar disponível em consultórios médicos e locais de varejo, como farmácias que administram outras vacinas.
Assim que a vacina estiver disponível, qualquer dose comprada pelo governo dos EUA será gratuita para seus cidadãos. Embora a vacina em si seja gratuita, a instituição ou agência que a oferece pode cobrar uma taxa pela administração. Os programas de saúde pública e planos de seguro devem reembolsar os pacientes por quaisquer custos associados à vacinação COVID-19, mas nenhuma informação foi disponibilizada ainda.
Efeitos colaterais e eventos adversos
Nenhum evento adverso sério foi relatado nos primeiros ensaios da vacina Novavax, mas mais informações estarão disponíveis após a publicação dos resultados do ensaio em estágio final. Na Fase 3, os eventos adversos "ocorreram em níveis baixos e foram equilibrados entre os grupos de vacina e placebo". de acordo com Novavax.
Financiamento e Desenvolvimento
A Novavax recebeu mais de US $ 2 bilhões globalmente por seus esforços para desenvolver uma vacina COVID-19, com US $ 1,6 bilhão somente do governo dos EUA. Os fundos dos EUA foram doados como parte da Operação Warp Speed e da Autoridade de Pesquisa e Desenvolvimento Avançado Biomédico (BARDA). BARDA é um programa que pertence ao Departamento de Saúde e Serviços Humanos dos Estados Unidos. Esse programa e a Operação Warp Speed procuraram acelerar a rapidez com que as vacinas para combater o COVID-19 podem ser desenvolvidas e aprovadas para uso.