
Imagens Pool / Pool / Getty
Principais vantagens
- O FDA concedeu autorização de uso emergencial para a vacina COVID-19 desenvolvida pela Pfizer e BioNTech.
- A notícia chega um dia depois que um comitê consultivo do FDA recomendou que a agência autorizasse a vacina
- Os dados revisados pelo comitê revelaram que a vacina é 95% eficaz.
- A distribuição das vacinas pode ocorrer dentro de 24 horas após a autorização.
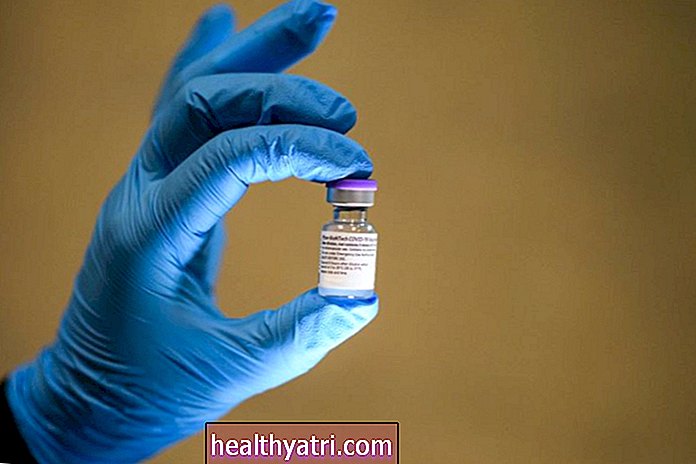
A Food and Drug Administration (FDA) concedeu autorização de uso de emergência para sua primeira vacina COVID-19 na noite de sexta-feira. A vacina, desenvolvida pela Pfizer Inc. e pela empresa alemã BioNTech, começará a ser distribuída em breve.
A notícia segue uma audiência pública muito esperada na quinta-feira, durante a qual um painel consultivo do FDA votou 17-4 a favor da autorização da vacina Pfizer, com uma abstenção.
A Pfizer apresentou dados de ensaios clínicos envolvendo 43.000 participantes adultos. No início desta semana, o FDA compartilhou alguns desses dados, incluindo o fato de que 95% das pessoas no ensaio clínico que receberam a vacina não desenvolveram COVID -19. Os efeitos colaterais foram menores, incluindo calafrios, dor leve e vermelhidão no local da injeção.
A autorização de uso de emergência (EUA) se aplica a pessoas com 16 anos ou mais. A Pfizer também está conduzindo testes clínicos sobre a segurança e eficácia da vacina em crianças a partir dos 12 anos, e espera-se que acrescente testes para crianças menores também.
Ainda são necessários dados de segurança e eficácia de mais populações
O painel consultivo da FDA, denominado Comitê Consultivo de Vacinas e Produtos Biológicos Relacionados (VRBPAC), recomenda que a Pfizer tome medidas adicionais para garantir que sua vacina seja segura e eficaz para mais populações. O painel recomenda que mais pessoas negras sejam adicionadas aos ensaios clínicos em andamento. Pessoas de cor têm maior probabilidade do que pessoas brancas de contrair COVID-19 e morrer do vírus.
O painel também discutiu dois casos relatados de reações alérgicas em pessoas que receberam a vacina no Reino Unido esta semana, onde ela já foi aprovada. Paul Offit, MD, diretor do Centro de Educação de Vacinas do Hospital Infantil da Filadélfia, perguntou aos apresentadores da Pfizer sobre as reações alérgicas, preocupado que pessoas com alergias graves optassem por não tomar a vacina. Offit recomendou que também fossem realizados estudos sobre a vacina em pessoas com alergias comuns.
O Reino Unido está recomendando que as pessoas com histórico de anafilaxia a um medicamento ou alimento não tomem a vacina. Os EUA podem adicionar um aviso semelhante em conjunto com a autorização. Funcionários da FDA na reunião disseram ao painel que já estavam trabalhando na documentação escrita para os consumidores sobre a segurança e eficácia da vacina.
O que isso significa para você
Com base na recomendação de um comitê consultivo para autorizar a vacina COVID-19 da Pfizer, a Food and Drug Administration pode aprovar seu uso em poucos dias. A distribuição pode começar logo depois disso. Espera-se que as primeiras doses da vacina sejam administradas a profissionais de saúde e residentes de lares de idosos.
Após a decisão do VRBPAC, o comissário da FDA Stephen M. Hahn, MD, emitiu uma declaração:
“Normalmente, o processo de revisão das vacinas estudadas em dezenas de milhares de pessoas leva meses. Embora o processo tenha sido acelerado em associação com a revisão deste EUA, a equipe de revisão de especialistas do FDA revisou milhares de páginas de informações técnicas [incluindo] dados de ensaios clínicos, dados não clínicos sobre o desenvolvimento da vacina em laboratório, e dados de fabricação sobre como a vacina é feita. ”
Hahn, provavelmente tentando acalmar os temores entre os consumidores, acrescentou: “Neste momento de grande urgência, a equipe da FDA sente a responsabilidade de avançar o mais rápido possível através do processo de revisão. No entanto, eles sabem que devem cumprir seu mandato de proteger a saúde pública e garantir que qualquer vacina autorizada atenda aos nossos rigorosos padrões de segurança e eficácia que o povo americano espera. ”
O presidente eleito Joe Biden também emitiu uma declaração após a votação do comitê dizendo: “a integridade da ciência nos levou a este ponto”.
O FDA afirma que a distribuição das vacinas pode ocorrer dentro de 24 horas após a autorização.
O comitê consultivo do FDA analisará uma segunda vacina COVID-19, feita pela Moderna, na quinta-feira, 17 de dezembro.

















.jpg)


