VioletaStoimenova / Getty Images
Principais vantagens
- O FDA está trabalhando em estreita colaboração com os fabricantes nos dados de segurança e eficácia que espera ver para considerar a aprovação de uma vacina COVID-19.
- O FDA planeja convocar um comitê consultivo externo para revisar os dados sobre cada vacina COVID-19 que arquiva para autorização.
- As empresas que obtêm uma autorização de uso de emergência para uma vacina COVID-19 devem continuar seus ensaios clínicos para fornecer informações de longo prazo sobre segurança e eficácia.
- O FDA espera que as empresas que recebem uma autorização de uso de emergência também solicitem uma aprovação padrão não emergencial.
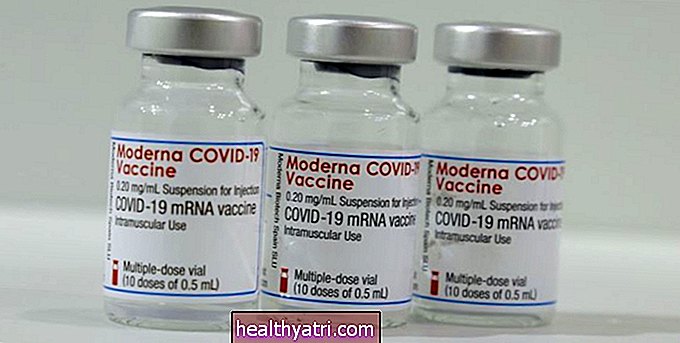
Hoje, o Food and Drug Administration (FDA) Administration convocou, pela segunda vez em uma semana, seu Comitê Consultivo de Vacinas e Produtos Biológicos Relacionados para recomendar uma “autorização de uso de emergência” (EUA) para uma nova vacina COVID-19 fabricada pela Moderna.
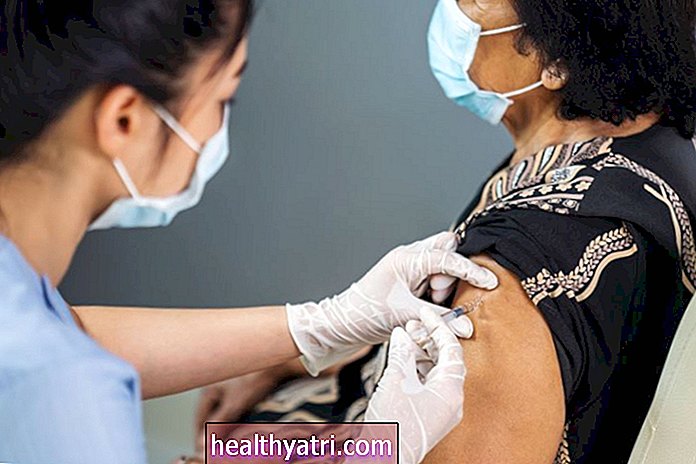
A primeira vacina COVID-19, feita pela Pfizer-BioNTech, foi autorizada pelo FDA na semana passada, e as vacinações de alguns profissionais de saúde - as primeiras pessoas designadas para receber a vacina - começaram nos EUA na segunda-feira passada.
Mas o que exatamente é um EUA?
O programa EUA foi estabelecido em 2004, após o ataque terrorista de 11 de setembro de 2001 nos EUA, para autorizar o uso de um produto médico não aprovado ou o uso não aprovado de um produto médico aprovado durante uma emergência declarada de saúde pública. COVID-19 foi estabelecido como uma emergência de saúde pública nos EUA pelo Secretário de Saúde e Serviços Humanos Alex Azar em 31 de janeiro de 2020.
Vacinas COVID-19: Mantenha-se atualizado sobre quais vacinas estão disponíveis, quem pode obtê-las e quão seguras são.
“Quando há uma emergência declarada, o FDA pode julgar que vale a pena liberar algo para uso, mesmo sem todas as evidências que estabeleceriam totalmente sua eficácia e segurança”, disse Joshua Sharfstein, um ex-comissário-adjunto principal do FDA. . Sharfstein é agora vice-reitor de Prática de Saúde Pública e Envolvimento Comunitário na Escola de Saúde Pública Johns Hopkins Bloomberg em Baltimore, Maryland.
As EUAs foram emitidas anteriormente para medicamentos ou vacinas para tratar ou prevenir o antraz, o ebola e a síndrome respiratória do Oriente Médio (MERS), diz Sharfstein.
Requisitos de aplicação EUA
Um fabricante pode solicitar uma EUA - ao contrário de uma aprovação mais formal para um pedido de licença biológica (BLA) - se não houver outra vacina disponível para prevenir a doença. Além disso, o FDA deve decidir que os benefícios conhecidos e potenciais da vacina superam os riscos de recebê-la.
“[Para um EUA] geralmente há menos dados do que estaria disponível para [um BLA]," LJ Tan, diretor de estratégia da Immunization Action Coalition, um grupo de defesa que trabalha para aumentar as taxas de imunização nos EUA, disse a Verywell "Mas isso não quer dizer que os ensaios clínicos estejam comprometidos em design. É apenas que o EUA é emitido antes do licenciamento, então não teremos tantos dados acumulados para o ensaio ainda."
De acordo com o FDA, os produtos submetidos a uma EUA ainda devem passar por testes rigorosos. Em outubro, o FDA compartilhou a orientação da indústria sobre o que estaria procurando em termos de dados de segurança e eficácia para as vacinas COVID-19, incluindo dados de estudos sobre a segurança da vacina, mais pelo menos dois meses de acompanhamento após o ensaio clínico conclusões.
De acordo com a orientação, o FDA pode conceder uma EUA para uma vacina se:
- O produto pode prevenir, diagnosticar ou tratar razoavelmente doenças ou condições graves ou potencialmente fatais que podem ser causadas pelo SARS-CoV-2.
- Os benefícios conhecidos e potenciais superam os riscos conhecidos e potenciais.
- Não há alternativa adequada, aprovada e disponível ao produto para diagnosticar, prevenir ou tratar a doença ou condição.
O FDA espera que os fabricantes de vacinas incluam um plano para acompanhar a segurança da vacina - que envolve a investigação de quaisquer relatórios de mortes, hospitalizações e outros eventos adversos graves ou clinicamente significativos - entre os indivíduos que recebem a vacina sob um EUA.
“Ser aberto e claro sobre as circunstâncias em que a emissão de uma autorização de uso de emergência para uma vacina COVID-19 seria apropriada é fundamental para construir a confiança do público e garantir o uso das vacinas COVID-19, uma vez disponíveis,” Peter Marks, MD, PhD, diretor do Centro de Avaliação e Pesquisa Biológica do FDA, disse em um comunicado. “Além de delinear nossas expectativas para os patrocinadores da vacina, também esperamos que a orientação da agência sobre as vacinas COVID-19 ajude o público a entender nosso processo de tomada de decisão com base científica que garante a qualidade, segurança e eficácia da vacina para qualquer vacina que seja autorizada ou aprovada . "
O FDA também espera que os fabricantes que recebem uma EUA continuem seus testes clínicos e, por fim, solicitem um BLA. Uma EUA não é mais válida uma vez que uma declaração de emergência de saúde pública não esteja mais em vigor, o que significa que a aprovação total será necessária para que a vacina continue a ser usada.
O que isso significa para você
A Food and Drug Administration está permitindo que as empresas solicitem autorização para COVID-19 sob um procedimento denominado autorização de uso de emergência, que pode acelerar o tempo que leva para obter a aprovação de uma vacina.