Getty Images
Principais vantagens
- Um novo estudo descobriu que o FDA tem um histórico de aprovação de opioides para uso com dados limitados.
- 81% dos dados aceitos pelo FDA excluíram pacientes que não toleraram a droga, tiveram efeitos colaterais ou não experimentaram benefícios.
- Muitos estudos aceitos para opioides projetados para uso em longo prazo foram curtos.
Um novo estudo descobriu que a Food and Drug Administration (FDA) tem um histórico de aprovação de opioides prescritos com dados limitados. Atualmente, os EUA estão em meio a uma crise de opioides.
O estudo, que foi publicado noAnnals of Internal Medicine, analisou dados de novos pedidos de medicamentos para opioides submetidos ao FDA entre 1997 e 2018. Os pesquisadores analisaram 48 novos pedidos de medicamentos, que eram em grande parte para novas dosagens de opioides ou novas formações.
Dos 39 novos pedidos de medicamentos que foram aprovados para o tratamento da dor crônica, apenas 21 tiveram pelo menos um ensaio fundamental para apoiar seu uso. A maioria dos ensaios durou em média 84 dias e envolveu cerca de 299 pacientes. Os pesquisadores descobriram que 81% dos medicamentos foram aprovados com base em desenhos de estudos que excluíram pacientes que não podiam tolerar os medicamentos, tinham efeitos colaterais ruins precoces ou não experimentaram muitos benefícios imediatos.
Cerca de 20% das novas aplicações de medicamentos para dor crônica agruparam análises de segurança, com sete deles relatando uso não médico e 15 relatando pacientes que desenvolveram tolerância ao medicamento.
Oito dos nove medicamentos que receberam a aprovação de um novo medicamento tiveram testes que duraram apenas um a dois dias e envolveram cerca de 329 pacientes.
“Entre 1997 e 2018, o FDA aprovou os opioides com base em testes essenciais de curta ou intermediária duração, muitas vezes em populações de dor estritamente definidas de pacientes que poderiam tolerar a droga”, escreveram os pesquisadores no artigo. “A comparação sistemática de resultados de segurança importantes era rara.”
Opioids Basics
Os opioides são uma classe de medicamentos usados para reduzir a dor, de acordo com os Centros de Controle e Prevenção de Doenças (CDC). Os opioides incluem o seguinte:
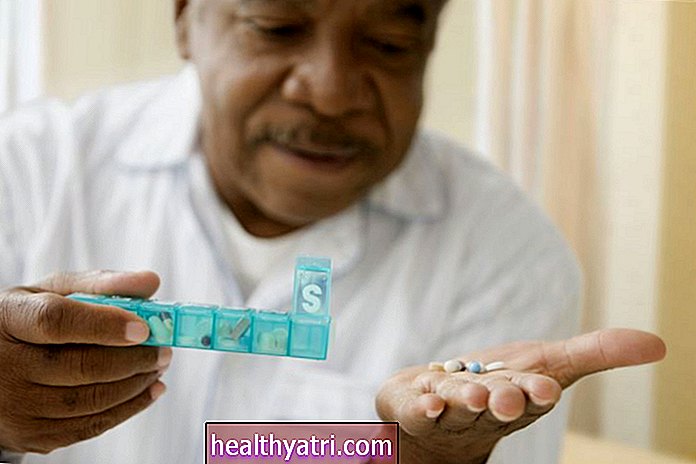
- Opioides prescritos: podem ser prescritos por médicos para tratar dores moderadas a fortes, mas também podem causar riscos e efeitos colaterais graves. Opioides de prescrição comuns incluem oxicodona (OxyContin), hidrocodona (Vicodin), morfina e metadona.
- Fentanil: um analgésico opioide sintético, o fentanil é muito mais poderoso do que outros opioides. É aprovado para o tratamento de dores fortes, geralmente dores associadas a câncer avançado. O fentanil também é feito e distribuído ilegalmente nos EUA.
- Heroína: Este é um opióide ilegal. Seu uso aumentou nos EUA.
A crise de opióides
O Instituto Nacional de Abuso de Drogas (NIDA) chama o uso indevido de opioides de uma "crise nacional séria", observando que o fardo econômico total do uso indevido de opioides prescritos é de US $ 78,5 bilhões por ano. Isso inclui os custos de saúde, perda de produtividade e tratamento de dependência e envolvimento do sistema de justiça criminal.
Os EUA enfrentam um número recorde de mortes por overdose de drogas. Em 2018, mais de 67.000 americanos morreram de overdose de drogas - desses, quase 70% envolviam opioides, diz o CDC.
O NIDA diz que a crise começou no final dos anos 1990, quando as empresas farmacêuticas garantiram à comunidade médica que os pacientes não se tornariam viciados em analgésicos opióides prescritos. Como resultado, os provedores de saúde começaram a prescrevê-los mais.
Logo ficou claro que os medicamentos podem ser altamente viciantes e as taxas de overdose de opioides aumentaram.
Agora, o NIDA diz que até 29% dos pacientes que recebem prescrição de opioides para dor crônica os usam indevidamente, e entre 8% e 12% desenvolveram um distúrbio devido ao uso de opioides. Até 6% dos que fazem uso indevido de opioides prescritos, fazem a transição para a heroína.
O papel do FDA na crise
“Apesar do escopo da epidemia de opioides em curso na América, pouco se sabe sobre a aprovação do FDA de novos produtos opioides nas últimas duas décadas”, co-autor do estudo Caleb Alexander, MD, professor de epidemiologia na Escola de Saúde Pública Johns Hopkins Bloomberg , diz Verywell.
Alexander cita muitos métodos usados pelo FDA como preocupantes, incluindo que “entre os testes de produtos aprovados para dor crônica, nenhum se estendeu além de 84 dias, apesar do fato de que muitos indivíduos tomam esses medicamentos por períodos muito mais longos de tempo”.
Alexander argumenta que o FDA poderia regular mais rigidamente os opioides antes de serem aprovados. “O FDA tem flexibilidade regulatória nos requisitos que definiu para acesso ao mercado, e nossas descobertas sugerem que a agência não usou isso para exigir que os fabricantes de opioides produzissem mais informações sobre a segurança e eficácia dos opioides prescritos antes da entrada no mercado”, diz ele. .
No futuro, Alexander diz que o FDA pode “melhorar a regulamentação dos opioides, exigindo que os fabricantes produzam mais e mais relevantes informações sobre a segurança e eficácia sistemáticas dos opioides”. Ele recomenda que o FDA exija que os fabricantes avaliem sistematicamente resultados ruins para a saúde associados ao uso de opioides, bem como parem de depender de testes "enriquecidos" que "dificilmente refletem a verdadeira eficácia do produto".
“O FDA também deve melhorar as orientações para os fabricantes, fornecendo explicitamente informações sobre as populações, a duração da terapia e os resultados de eficácia e segurança que devem ser medidos em testes futuros”, diz Alexander.
Finalmente, Alexander diz, “o FDA também deve rotular novamente os opioides crônicos para que a rotulagem desses produtos importantes reflita melhor as condições sob as quais foram estudados para aprovação regulatória”
O que isso significa para você
O abuso de opióides prescritos continua sendo um problema nos EUA, onde o FDA tem um histórico de aprovação de medicamentos com base em dados limitados de curto prazo. Se você recebeu prescrição de opioides para a dor, converse com seu médico sobre o potencial para vício e efeitos colaterais graves.
Em 2018, o FDA divulgou um Roteiro de Política Estratégica no qual a agência prometeu garantir melhores práticas de prescrição, apoiar o tratamento de pessoas viciadas em opioides e aumentar os esforços para impedir o embarque ilegal de opioides para o país. O FDA também diz que planeja tomar medidas para ajudar com tratamentos alternativos para a dor crônica.
O FDA divulgou um cronograma público de “atividades selecionadas” e “eventos significativos” elaborado para lidar com o uso indevido e abuso de opioides. Mais recentemente, a agência aprovou o Olinvyk (oliceridina), um opióide desenvolvido para o tratamento da dor aguda moderada a intensa em adultos.