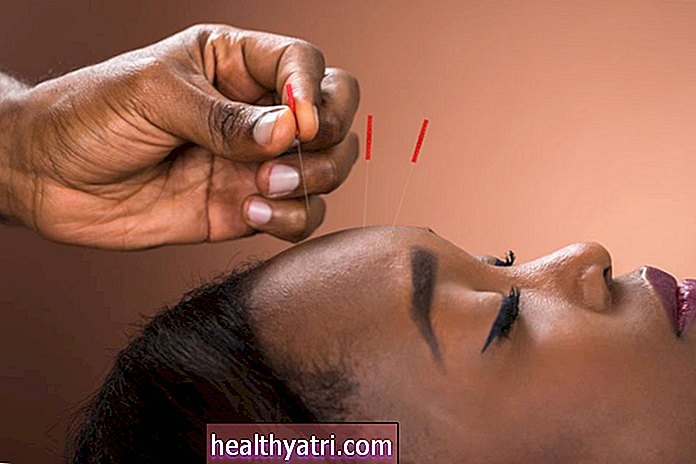
Apesar de mais de 35 anos de pesquisa, os cientistas ainda precisam encontrar uma cura para o vírus da imunodeficiência humana (HIV): o vírus que causa a síndrome da imunodeficiência adquirida (AIDS).
A terapia antirretroviral (ART) foi um grande avanço que ajuda a suprimir o vírus, mas não é uma cura. E embora tenha havido alguns casos bem divulgados em que o HIV foi dito ter sido curado - incluindo o de Timothy Brown, também conhecido como o paciente de Berlim - ainda não existe uma abordagem que possa erradicar o HIV de forma consistente e segura em uma base individual , muito menos em escala global. Mesmo assim, o progresso está sendo feito.
BIBLIOTECA DE FOTOS TEK IMAGE / SCIENCE / Getty Images
Desafios
Existem várias razões pelas quais encontrar uma cura para o HIV / AIDS tem sido um longo caminho de desafio após desafio. O HIV é um vírus tão complexo, multifacetado e em constante mutação que é difícil acompanhá-lo.
Alguns dos atuais desafios gerais enfrentados pela pesquisa em HIV incluem:
- Alcançando as populações com maior risco de infecção e transmissão do HIV
- Garantir que a pesquisa ocorra com o consentimento totalmente informado dos participantes, o que significa que eles compreendem totalmente os riscos e benefícios do ensaio
- Desenvolvimento de vacinas candidatas ao HIV seguras e eficazes para serem testadas por meio de ensaios clínicos com primatas humanos e não humanos
- Obter uma melhor compreensão dos mecanismos de resposta imunológica em humanos
- Levando as comorbidades do HIV em consideração na pesquisa, então qualquer cura potencial beneficiaria o maior número de pessoas possível
- Foco crescente no estudo de remissão observada em pacientes raros que interromperam o tratamento
- Definindo exatamente o que significa uma "cura" para o HIV
- Diminuir o estigma que ainda cerca o HIV, com o objetivo de minimizar seu impacto na participação em pesquisas sobre HIV
- Obter uma melhor compreensão de como tratar efetivamente as coinfecções por HIV e gerenciar as falhas de tratamento
Redução de transmissão
Embora não seja uma "cura", por si só, a estratégia de "tratamento como prevenção" (TasP) - envolvendo tomar medicação diária para o HIV - tem sido altamente eficaz na redução da transmissão para aqueles que já são HIV-positivos.
Além disso, em 2020, foi anunciado que a expectativa de vida das pessoas com HIV nos Estados Unidos era a mesma daqueles que nunca foram infectados com o vírus - embora tivessem muito menos anos de boa saúde.
Idealmente, o próximo passo será o desenvolvimento de uma vacina segura e eficaz contra o HIV, mas existem alguns desafios que impedem o progresso da pesquisa.
Variabilidade Genética
Um dos obstáculos mais significativos para a criação de uma vacina contra o HIV amplamente eficaz é a diversidade genética e a variabilidade do próprio vírus.
O desafio do ciclo de replicação
Em vez de ser capaz de se concentrar em uma única cepa do HIV, os pesquisadores precisam levar em conta o fato de que ele se replica tão rapidamente, o que pode causar mutações e novas cepas. O ciclo de replicação do HIV leva um pouco mais de 24 horas.
E embora o processo de replicação seja rápido, não é o mais preciso - produzindo muitas cópias mutadas a cada vez, que então se combinam para formar novas cepas conforme o vírus é transmitido entre pessoas diferentes.
Por exemplo, no HIV-1 (uma única cepa de HIV), existem 13 subtipos e subtipos distintos que estão ligados geograficamente, com variação de 15% a 20% dentro dos subtipos e variações de até 35% entre os subtipos.
Não apenas isso é um desafio na criação de uma vacina, mas também porque algumas das cepas mutadas são resistentes à TARV, o que significa que algumas pessoas têm mutações mais agressivas do vírus.
Reservatórios latentes
Além das cepas de HIV em constante evolução e mutação, outro desafio no desenvolvimento de uma vacina é algo chamado de reservatórios latentes. Eles são estabelecidos durante o estágio inicial da infecção pelo HIV e podem efetivamente “ocultar” o vírus da detecção imunológica, bem como os efeitos da TARV.
Isso significa que, se o tratamento for interrompido, uma célula infectada latentemente pode ser reativada, fazendo com que a célula comece a produzir o HIV novamente.
Embora o ART possa suprimir os níveis de HIV, não pode eliminar os reservatórios latentes de HIV - o que significa que o ART não pode curar a infecção pelo HIV.
Esgotamento Imunológico
Há também o desafio da exaustão imunológica que acompanha uma infecção de HIV de longo prazo. Esta é a perda gradual da capacidade do sistema imunológico de reconhecer o vírus e lançar uma resposta apropriada.
Qualquer tipo de vacina contra o HIV, cura da AIDS ou outro tratamento deve ser criado levando-se em consideração a exaustão imunológica, encontrando maneiras de abordar e compensar as capacidades decrescentes do sistema imunológico de uma pessoa ao longo do tempo.
Progresso Inicial
Embora o progresso feito para a cura do HIV tenha sido lento, ainda há vislumbres de esperança ao longo do caminho, indicando que os cientistas podem estar se aproximando de um tratamento amplamente eficaz.
O paciente berlinense
Talvez o caso mais conhecido até agora tenha sido o de Timothy Brown, também conhecido como "o paciente de Berlim", considerado a primeira pessoa a ser "curada funcionalmente" do HIV.
Apesar de seu apelido, Brown nasceu nos Estados Unidos, mas foi diagnosticado com HIV em 1995 enquanto estudava na Alemanha. Dez anos depois, ele foi diagnosticado com leucemia mieloide aguda (LMA) e precisou de um transplante de células-tronco para ter alguma chance de sobreviver ao câncer.
Quando os médicos descobriram que Brown combinava com 267 doadores (muitas pessoas não encontram um único compatível), eles decidiram usar um que tinha uma mutação chamada CCR5-delta 32, considerada capaz de induzir imunidade ao HIV.
Três meses após o transplante de fevereiro de 2007, o HIV não foi mais detectado no sangue de Brown. E embora ele continuasse a ter complicações com leucemia - e necessitasse de transplantes adicionais de células-tronco - a infecção de Brown pelo HIV não voltou. Esse foi o caso até sua morte em 2020 de leucemia.
Os médicos do Brigham and Women's Hospital em Boston tentaram usar uma técnica de transplante de células-tronco semelhante em dois pacientes entre 2008 e 2012 - embora sem usar doadores com a mutação delta 32. Embora os pacientes inicialmente experimentassem 10 e 13 meses de níveis indetectáveis de HIV, ambos passaram posteriormente por um rebote viral.
O paciente londrino
Um estudo de 2019 foi publicado fornecendo detalhes sobre uma segunda pessoa - Adam Castillejo, desta vez conhecido como "o Paciente de Londres" - que também parece ter sido funcionalmente curado do HIV.
Sua situação era semelhante à de Brown, pois ele tinha câncer, recebeu quimioterapia para eliminar seu sistema imunológico e, em seguida, fez um transplante de células-tronco usando células de um doador com uma mutação genética que leva à imunidade ao HIV.
Até agora, há evidências clínicas de que Castillejo está em remissão do HIV-1 há 30 meses sem nenhum vírus competente para replicação detectável, embora não esteja claro se isso vai continuar.
E embora o uso de um transplante de células-tronco para produzir imunidade ao HIV possa ter sido bem-sucedido para Brown e Castillejo, não é algo que será usado em sua forma atual na prática clínica regular tão cedo.
Esse processo de várias etapas não é apenas caro, mas também envolve muitos riscos e danos potenciais para o paciente.
Como Brown e Castillejo tinham câncer e precisavam de um transplante de células-tronco, encontrar um doador com a mutação delta 32 fazia sentido. No entanto, não é uma opção viável para alguém sem câncer se submeter a esse tratamento específico.
Apesar das limitações práticas do tratamento, esses casos ofereceram aos cientistas insights que avançaram as pesquisas sobre a cura do HIV de maneiras significativas.
Terapia genética baseada em células-tronco
Um tipo de tratamento que mostra potencial inicial é a terapia genética baseada em células-tronco - uma abordagem amplamente informada pelo caso de Brown.
Seu objetivo é reconstituir uma pessoa com o sistema imunológico do HIV através do transplante de células-tronco hematopoéticas geneticamente modificadas com genes anti-HIV, que podem não apenas se auto-renovar, mas também podem se multiplicar e se diferenciar em células imunológicas maduras.
Tem havido algum sucesso nas primeiras pesquisas em terapia genética baseada em células-tronco.
Um estudo de 2018 envolvendo macacos pigtail infectados com HIV descobriu que um transplante de células-tronco editadas por genes foi capaz de reduzir significativamente o tamanho de seus "reservatórios virais" dormentes que poderiam ser reativados para produzir cópias adicionais do vírus.
Progresso adicional foi feito desde então com primatas. De acordo com um estudo de 2021, os pesquisadores determinaram uma fórmula que poderia prever a dose ideal de células-tronco necessária para curar o HIV.
Ainda trabalho a ser feito
Embora a abordagem tenha se mostrado promissora em primatas, não é de forma alguma replicável em escala global.
Agora, o objetivo é replicar os efeitos dos transplantes de células-tronco de Brown e Castillejo em outros humanos, mas sem a toxicidade de ter que se submeter à quimioterapia primeiro.
Anticorpos amplamente neutralizantes
Alguns dos modelos de vacina mais promissores até o momento envolvem anticorpos amplamente neutralizantes (bNAbs) - um tipo raro de anticorpo que é capaz de atingir a maioria das variantes do HIV.
Os BNAbs foram descobertos pela primeira vez em vários controladores de elite do HIV - pessoas que parecem ter a capacidade de suprimir a replicação viral sem ART e não mostram nenhuma evidência de progressão da doença. Alguns desses anticorpos especializados, como o VRC01, são capazes de neutralizar mais de 95% das variantes do HIV.
Atualmente, os pesquisadores de vacinas estão tentando estimular a produção de bNAbs.
Um estudo de 2019 envolvendo macacos se mostra promissor. Depois de receber uma única injeção de vacina contra o HIV, seis dos 12 macacos no teste desenvolveram anticorpos que retardaram significativamente a infecção e, em dois casos, até a preveniram.
bNAbs mostrando promessa
Essa abordagem ainda está nos estágios iniciais de testes em humanos, embora em março de 2020 tenha sido anunciado que, pela primeira vez, os cientistas foram capazes de desenvolver uma vacina que induziu células humanas a gerar bNAbs.
Este é um desenvolvimento notável, após anos de estudos anteriores, que, até o momento, foram bloqueados pela falta de uma resposta de bNAb robusta ou específica.
Reversão de latência
Até que os cientistas consigam “limpar” os reservatórios latentes do HIV, é improvável que qualquer vacina ou abordagem terapêutica erradique totalmente o vírus.
Alguns agentes, incluindo inibidores de HDAC usados na terapia do câncer, mostraram-se promissores, mas ainda não foram capazes de atingir altos níveis de depuração sem risco de toxicidade. Além disso, os cientistas não têm certeza de quão extensos esses reservatórios realmente são.
Ainda assim, espera-se que a combinação de um agente de reversão de latência com uma vacina (ou outros agentes esterilizantes) possa ter sucesso com uma estratégia experimental curativa conhecida como "chutar e matar" (também conhecido como "choque e matar") que está atualmente sob investigação.
Estratégia Kick-and-Kill
É um processo de duas etapas:
- Primeiro, os medicamentos chamados agentes de reversão da latência são usados para reativar o HIV latente escondido nas células do sistema imunológico (a parte "chute" ou "choque").
- Então, uma vez que as células imunológicas são reativadas, o sistema imunológico do corpo - ou drogas anti-HIV - pode atingir e matar as células reativadas.
Infelizmente, os agentes de reversão da latência por si só não são capazes de reduzir o tamanho dos reservatórios virais.
Outra estratégia de reversão de latência pode envolver inibidores de PD-1 como Keytruda (pembrolizumabe), que se mostraram promissores em limpar os reservatórios virais, ao mesmo tempo que revertem potencialmente a exaustão imunológica.
PD-1 atua como um ponto de verificação imunológico e é expresso preferencialmente na superfície de células infectadas de forma persistente. Mas, neste ponto, ainda não está claro se o PD-1 desempenha um papel funcional na latência do HIV e na persistência do reservatório.
Uma palavra de Verywell
Embora haja progresso em direção à cura do HIV, é muito cedo para dizer quando um avanço pode ocorrer.
Felizmente, os cientistas fizeram grandes avanços na prevenção do HIV - particularmente por meio da profilaxia pré-exposição (ou PrEP). A ideia por trás da PrEP é dar às pessoas com alto risco de contrair o HIV, mas não infectadas, a oportunidade de evitar que isso aconteça tomando um comprimido uma vez ao dia. Quando usada correta e consistentemente, a PrEP reduz o risco de contrair o HIV por meio do sexo em cerca de 99% e de drogas injetáveis em 74%.
Mas até que a cura seja encontrada, o melhor resultado para as pessoas com HIV é a terapia anti-retroviral, que pode reduzir o risco de doenças associadas ao HIV e manter a expectativa de vida - para os que vivem nos Estados Unidos - em uma duração semelhante à daqueles que não o fazem tem HIV.
.jpg)






.jpg)






-side-effects.jpg)